Correlations of cerebrospinal fluid CTHRC1 and OLFM3 levels with cognitive impairment and cerebrospinal fluid biomarkers in patients with Alzheimer′s disease
-
摘要:目的
探讨阿尔茨海默病(AD)患者脑脊液胶原三螺旋重复蛋白-1(CTHRC1)、溴素结构域家族蛋白3(OLFM3)水平与其认知功能损害以及脑脊液生物标志物水平的关系。
方法选取96例AD患者为研究对象(AD组),根据临床痴呆量表(CDR)评分分为轻度组(n=34)、中度组(n=39)和重度组(n=33)。选取同期行腰椎穿刺检查的非认知功能障碍患者60例为对照组。采用酶联免疫吸附法检测脑脊液CTHRC1、OLFM3水平以及脑脊液标志物[β-淀粉样蛋白(Aβ)-40、Aβ-42、Aβ42/Aβ-40、总tau蛋白(T-tau)和磷酸化tau蛋白(P-tau)]水平。采用简易精神状态量表(MMSE)和蒙特利尔认知评估量表(MoCA)评估AD患者的认知功能损害情况。分析脑脊液CTHRC1、OLFM3水平与认知功能损害及脑脊液标志物的关系。
结果AD组脑脊液CTHRC1、T-tau和P-tau高于对照组, OLFM3、Aβ-42和Aβ-42/Aβ-40低于对照组,差异有统计学意义(P < 0.05)。脑脊液CTHRC1和OLFM3诊断AD的曲线下面积(AUC)分别为0.839、0.822, 其联合诊断的AUC为0.923。轻度组、中度组、重度组的脑脊液CTHRC1依次升高, OLFM3依次降低,差异有统计学意义(P < 0.05)。轻度组、中度组、重度组的脑脊液Aβ-42及Aβ-42/Aβ-40依次降低, T-tau及P-tau依次升高,差异有统计学意义(P < 0.05)。轻度组、中度组、重度组的MMSE、MoCA评分依次降低,差异有统计学意义(P < 0.05)。AD患者脑脊液CTHRC1与病情严重程度呈正相关, OLFM3与病情严重程度呈负相关(P < 0.05)。脑脊液CTHRC1与Aβ-42、Aβ-42/Aβ-40、MMSE评分和MoCA评分呈负相关, 与T-tau、P-tau呈正相关(P < 0.05)。脑脊液OLFM3与Aβ-42、Aβ-42/Aβ-40、MMSE评分和MoCA评分呈正相关,与T-tau、P-tau呈负相关(P < 0.05)。
结论AD患者脑脊液中CTHRC1升高, OLFM3降低。CTHRC1、OLFM3与AD病情严重程度、认知功能损害以及脑脊液标志物水平有关。
-
关键词:
- 阿尔茨海默病 /
- 胶原三螺旋重复蛋白-1 /
- 溴素结构域家族蛋白3 /
- 认知功能 /
- 脑脊液生物标志物 /
- 神经元
Abstract:ObjectiveTo investigate the relationships of cerebrospinal fluid levels of collagen triple helix repeat containing-1 (CTHRC1) and olfactomedin-3 (OLFM3) with cognitive impairment and cerebrospinal fluid biomarker levels in patients with Alzheimer′s disease (AD).
MethodsNinety-six patients with AD were selected as study objects (AD group), and divided into mild group (n=34), moderate group (n=39) and severe group (n=33) according to Clinical Deentia Scale (CDR) score. Sixty patients without cognitive impairment who underwent lumbar puncture during the same period served as the control group. Enzyme-linked immunosorbent assays were used to measure cerebrospinal fluid levels of CTHRC1, OLFM3 and biomarkers [β-amyloid (Aβ)-40, Aβ-42, Aβ42/Aβ-40, total tau (T-tau) and phosphorylated tau (P-tau)]. Cognitive impairment in AD patients was assessed using the Mini-Mental State Examination (MMSE) and Montreal Cognitive Assessment (MoCA). The relationships of CSF CTHRC1 and OLFM3 levels with cognitive impairment and cerebrospinal fluid biomarkers were analyzed.
ResultsThe AD group showed significantly higher cerebrospinal fluid levels of CTHRC1, T-tau and P-tau, and significantly lower levels of OLFM3, Aβ-42 and Aβ42/Aβ-40 compared to the control group (P < 0.05). The area under the curve (AUC) for diagnosing AD with cerebrospinal fluid CTHRC1 and OLFM3 was 0.839 and 0.822, respectively, and the combined AUC was 0.923. Cerebrospinal fluid CTHRC1 of mild group, moderate group and severe group were increased successively, and OLFM3 was decreased successively, the difference was statistically significant (P < 0.05). Cerebrospinal fluid Aβ-42 and Aβ-42/Aβ-40 in mild, moderate and severe groups were decreased successively, while T-tau and P-tau were increased successively, with statistical significance (P < 0.05). The MMSE and MoCA scores of mild group, moderate group and severe group decreased successively, and the difference was statistically significant (P < 0.05). Cerebrospinal fluid CTHRC1 levels were positively correlated with disease severity, while OLFM3 levels were negatively correlated (P < 0.05). Cerebrospinal fluid CTHRC1 was negatively correlated with Aβ-42, Aβ42/Aβ-40, MMSE scores and MoCA scores, and positively correlated with T-tau and P-tau (P < 0.05). Cerebrospinal fluid OLFM3 was positively correlated with Aβ-42, Aβ42/Aβ-40, MMSE scores and MoCA scores, and negatively correlated with T-tau and P-tau (P < 0.05).
ConclusionIn the cerebrospinal fluid of patients with AD, CTHRC1 is elevated while OLFM3 is decreased. Both CTHRC1 and OLFM3 are associated with the severity of AD, cognitive impairment and levels of cerebrospinal fluid biomarkers.
-
阿尔茨海默病(AD)是一种复杂的神经系统退行性病变,主要表现为认知功能损害和记忆力渐进性衰退[1]。AD尚无有效治愈方法,早期诊断及评估认知功能损害程度,并实施精准治疗,是延缓病情进展的重要手段[2]。AD主要病理改变为β-淀粉样蛋白(Aβ)沉积及过度磷酸化tau蛋白(P-tau)形成的神经原纤维缠结,并伴有炎性因子激活和氧化应激反应增强[3]。胶原三螺旋重复蛋白1(CTHRC1)参与了机体损伤后的血管重塑修复及炎症反应过程[4], 其表达上调损伤线粒体功能,可引起Aβ肽血管沉积,导致淀粉样血管病变[5]。溴素结构域家族蛋白(OLFM3)表达下调可致神经元功能异常和突触损害,影响突触功能而致记忆和认知功能下降[6], 并与炎症反应密切相关,而炎症是AD进展的重要驱动因素[7]。关于CTHRC1和OLFM3与AD发病关系的研究,现有证据尚不充分。本研究探讨AD患者脑脊液CTHRC1、OLFM3表达水平及其与认知功能损害、脑脊液生物标志物的关系,现报告如下。
1. 资料与方法
1.1 一般资料
选取2018年8月—2023年8月榆林市星元医院收治的96例确诊AD患者(AD组)为研究对象。纳入标准: ①符合《2018中国痴呆与认知障碍诊治指南(二): 阿尔茨海默病诊治指南》[8]者; ②年龄≥18岁者; ③患者及其家属签署知情同意书。排除标准: ①心脏功能不全及肝、肾功能障碍者; ②急慢性炎症反应性疾病及自身免疫性疾病者; ③帕金森综合征、血管性痴呆、额颞叶痴呆等类型痴呆者; ④中风、精神分裂、抑郁症等脑部疾病者; ⑤恶性肿瘤者; ⑥其他研究者认为需要排除者。AD组中男55例,女41例; 年龄53~82岁,平均(75.22±8.15)岁; 体质量指数(BMI)为20~26 kg/m2, 平均(22.73±2.60) kg/m2; 文盲15例,小学26例,中学及以上55例。根据临床痴呆评定量表(CDR)简体中文版[9], 将患者分为轻度组(1分)34例,中度组(2分)39例和重度组(3分)23例。同期随机选取60例性别、年龄与AD组相近的行腰椎穿刺检查的非认知功能障碍患者为对照组。对照组中男32例,女28例; 年龄50~79岁,平均(74.31±8.67)岁; BMI为21~25 kg/m2, 平均(22.05±2.46) kg/m2; 文盲9例,小学26例,中学及以上25例; 紧张性头痛22例,面神经炎17例,周围神经病21例。AD组与对照组性别(χ2=0.235, P=0.628)、年龄(t=0.662, P=0.509)、BMI(t=1.625, P=0.107)、文化程度(χ2=4.692, P=0.96)比较,差异无统计学意义,具有可比性。本研究符合《赫尔辛基》宣言,且已获得医院伦理委员会批准(批号: 20180207002)。
1.2 方法
1.2.1 脑脊液CTHRC1、OLFM3及标志物检测
AD组和对照组均禁食12 h后,由经验丰富的神经内科医师次日在2组清晨空腹状态下行腰椎穿刺术,采集5 mL透明清亮的脑脊液于聚丙烯管中。以2 000 r/min离心10 min, 保留上清液并分成200 μL等份,保存于-80 ℃冰箱中待检。采用酶联免疫吸附法检测CTHRC1、OLFM3水平,CTHRC1酶联免疫试剂盒由上海瑞番生物公司提供, OLFM3酶联免疫试剂盒由上海酶联生物科技有限公司提供。同时采用酶联免疫吸附法检测2组患者的脑脊液标志物,包括Aβ-40、Aβ-42和两者比值(Aβ-42/Aβ-40)以及总tau蛋白(T-tau)、P-tau(Serine396), 酶联免疫试剂盒为INNOTEST试剂盒,均由日本Fujirebio公司提供。检测过程严格按照试剂盒说明书进行。
1.2.2 认知功能损害评估
在AD患者精神状态良好情况下,采用简易精神状态量表(MMSE)[10]及蒙特利尔认知评估量表(MoCA)[11]进行认知功能评估。MMSE评估内容包括定向力、回忆力、记忆力、注意力、计算力、语言和视空间能力,总分30分,得分 < 27分表明认知功能障碍,且得分越低表示认知功能损害越严重; MoCA评估内容包括视空间和执行功能、抽象、记忆、延迟回忆、注意、定向、命名和语言,总分30分,得分 < 26分表明认知功能异常,且得分越低表示认知功能损害越严重。
1.3 统计学分析
采用SAS 9.4软件分析数据。定量资料满足正态分布以(x±s)表示,多组比较采用单因素方差分析,多重比较采用Dunnett-t检验, 2组比较采用成组t检验; 定性资料以[n(%)]表示,比较采用χ2检验。绘制受试者工作特征(ROC)曲线并计算曲线下面积(AUC), 评估脑脊液CTHRC1、OLFM3对AD的诊断价值,采用Z检验比较不同指标间的诊断价值。采用Pearson积矩相关或Spearman秩相关分析法分析CTHRC1、OLFM3与AD患者病情严重程度及脑脊液标志物的关系。P < 0.05表示差异有统计学意义。
2. 结果
2.1 2组患者脑脊液CTHRC1、OLFM3及脑脊液标志物水平比较
AD组脑脊液CTHRC1水平高于对照组, OLFM3水平低于对照组,差异有统计学意义(P < 0.05); AD组脑脊液Aβ-42、Aβ-42/Aβ-40低于对照组, T-tau、P-tau水平高于对照组,差异有统计学意义(P < 0.05)。见表 1。
表 1 2组患者脑脊液的CTHRC1、OLFM3水平及脑脊液标志物(x±s)指标 AD组(n=96) 对照组(n=60) t P CTHRC1/(μg/L) 35.02±5.89 27.67±5.14 7.952 < 0.001 OLFM3/(μg/mL) 12.64±2.89 17.15±3.37 8.895 < 0.001 Aβ-40/(pg/mL) 7 265.89±1 622.70 6 826.40±1 357.51 1.753 0.082 Aβ-42/(pg/mL) 304.78±114.05 467.16±135.83 8.034 < 0.001 Aβ-42/Aβ-40 0.04±0.02 0.09±0.02 15.192 < 0.001 T-tau/(pg/mL) 513.75±122.38 159.75±103.43 18.634 < 0.001 P-tau/(pg/mL) 79.56±22.64 51.02±17.92 8.279 < 0.001 CTHRC1: 胶原三螺旋重复蛋白-1; OLFM3: 溴素结构域家族蛋白3; Aβ-40: β-淀粉样蛋白-40;
Aβ-42: β-淀粉样蛋白-42; T-tau: 总tau蛋白; P-tau: 磷酸化tau蛋白。2.2 脑脊液CTHRC1、OLFM3对AD患者的诊断价值
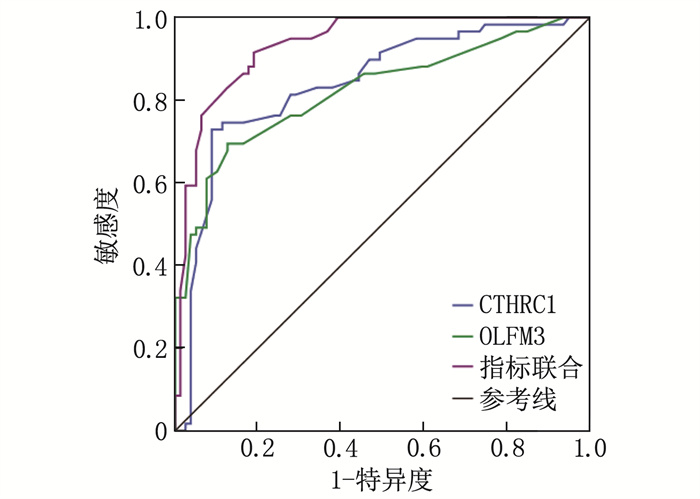
以AD患者为阳性样本,对照组患者为阴性样本,绘制ROC曲线,结果显示脑脊液CTHRC1、OLFM3诊断AD的AUC分别为0.839、0.822。指标联合拟合Logistic回归并得到返回概率Logit(P), 将其作为检验变量构建诊断模型, AUC为0.923, 联合诊断价值大于单一指标(Z=2.015、2.326,P=0.003、0.001)。见表 2和图 1。
表 2 脑脊液CTHRC1、OLFM3对AD患者的诊断价值指标 AUC 标准误 P 截断值 灵敏度 特异度 CTHRC1 0.839 0.036 < 0.001 32.18 μg/L 0.83 0.62 OLFM3 0.822 0.038 < 0.001 15.02 μg/mL 0.81 0.61 指标联合 0.923 0.021 < 0.001 — 0.95 0.77 2.3 不同病情严重程度AD患者的脑脊液CTHRC1、OLFM3及脑脊液标志物水平比较
重度组、中度组脑脊液CTHRC1水平高于轻度组,且重度组高于中度组,差异有统计学意义(P < 0.05); 重度组、中度组脑脊液OLFM3水平低于轻度组,且重度组低于中度组,差异有统计学意义(P < 0.05)。重度组、中度组脑脊液Aβ-42、Aβ-42/Aβ-40低于轻度组,且重度组低于中度组,差异有统计学意义(P < 0.05); 重度组、中度组脑脊液T-tau、P-tau水平高于轻度组,且重度组高于中度组,差异有统计学意义(P < 0.05)。见表 3。
表 3 不同病情严重程度AD患者的脑脊液CTHRC1、OLFM3及脑脊液标志物水平(x±s)指标 轻度组(n=34) 中度组(n=39) 重度组(n=23) F P CTHRC1/(μg/L) 27.91±6.11 32.64±6.89* 49.57±7.30*# 75.235 < 0.001 OLFM3/(μg/mL) 15.81±3.04 11.58±2.79* 9.76±2.51*# 36.241 < 0.001 Aβ-40/(pg/mL) 7 231.38±1 595.10 7 268.25±1 620.07 7 312.91±1 613.34 0.018 0.982 Aβ-42/(pg/mL) 356.91±70.76 295.32±65.82* 243.76±61.92*# 20.379 < 0.001 Aβ-42/Aβ-40 0.06±0.02 0.03±0.01* 0.02±0.01*# 63.935 < 0.001 T-tau/(pg/mL) 460.89±86.97 519.23±93.41* 582.61±97.29*# 12.089 < 0.001 P-tau/(pg/mL) 67.77±20.43 80.13±22.38* 96.02±23.91*# 11.240 < 0.001 与轻度组比较, *P < 0.05; 与中度组比较, #P < 0.05。 2.4 不同病情严重程度AD患者MMSE、MoCA评分比较
重度组、中度组的MMSE、MoCA评分低于轻度组,且重度组低于中度组,差异有统计学意义(P < 0.05)。见表 4。
表 4 不同病情严重程度AD患者的MMSE、MoCA评分(x±s)分指标 轻度组(n=34) 中度组(n=39) 重度组(n=23) F P MMSE评分 25.34±5.02 21.03±4.87* 16.39±4.26*# 24.214 < 0.001 MoCA评分 25.59±4.68 21.72±4.13* 15.45±3.89*# 38.528 < 0.001 与轻度组比较, *P < 0.05; 与中度组比较, #P < 0.05。 2.5 AD患者脑脊液的CTHRC1、OLFM3水平与病情严重程度及脑脊液标志物的关系
Spearman秩相关分析结果显示, AD患者脑脊液CTHRC1与病情严重程度呈正相关, OLFM3与病情严重程度呈负相关(P < 0.05)。脑脊液CTHRC1与Aβ-42、Aβ-42/Aβ-40以及MMSE、MoCA评分呈负相关,与T-tau、P-tau呈正相关(P < 0.05); 脑脊液OLFM3与Aβ-42、Aβ-42/Aβ-40以及MMSE、MoCA评分呈正相关,与T-tau、P-tau呈负相关(P < 0.05)。见表 5。
表 5 AD患者脑脊液CTHRC1、OLFM3水平与病情严重程度及脑脊液标志物的关系指标 CTHRC1 OLFM3 r或rs(95%CI) P r或rs(95%CI) P 病情严重程度 0.596(0.533~0.652) 0.001 -0.576(-0.627~-0.509) 0.003 Aβ-40 0.153(0.076~0.261) 0.349 0.229(0.101~0.375) 0.627 Aβ-42 -0.615(-0.661~-0.572) < 0.001 0.594(0.138~0.282) < 0.001 Aβ-42/Aβ-40 -0.639(-0.690~-0.594) < 0.001 0.601(0.568~0.654) < 0.001 T-tau 0.560(0.517~0.618) 0.003 -0.532(-0.579~-0.498) 0.005 P-tau 0.593(0.538~0.649) 0.002 -0.540(-0.591~-0.503) 0.004 MMSE评分 -0.627(-0.695~-0.572) < 0.001 0.597(0.534~0.649) < 0.001 MoCA评分 -0.641(-0.702~-0.599) < 0.001 0.611(0.568~0.673) 0.001 3. 讨论
AD在老年人群中发病率较高。2020年,中国60岁以上人口中,患病人数达到983万[12-15]。脑组织中Aβ蛋白沉积,激活小胶质细胞释放炎性因子,诱发神经炎症,导致神经细胞凋亡及神经退行性变,通过激活细胞周期蛋白依赖性激酶4引起Tau蛋白过度磷酸化,导致神经纤维缠结,信号转导和突触传递受阻,加速神经细胞退化和凋亡[16-20]。
CTHRC1通过促进成纤维样滑膜细胞迁移及血管形成,介导类风湿性关节炎血管翳形成[21]。CTHRC1也是线粒体损伤标志物, AD小鼠模型线粒体功能障碍引起Aβ肽血管沉积,并形成淀粉样血管病变,导致CTHRC1穿透血脑屏障进入血循环[6]。CTHRC1还可引起细胞外淀粉样斑块沉积,加速AD进展,激活Wnt信号通路促进β-连环蛋白表达,诱发并加重AD[22-23]。本研究发现,脑脊液CTHRC1表达上调可能参与AD发病过程。AD患者脑组织神经炎症刺激机体,释放CTHRC1参与炎症反应调控[24]; AD患者线粒体损伤通过氧化应激、线粒体功能障碍及膜通透性改变等途径影响神经细胞生理功能,加剧病情进展,线粒体损伤同时会引起细胞内氧化应激和内质网应激,促使细胞产生CTHRC1等应激蛋白[25]。CTHRC1表达上调还可促进淀粉样蛋白聚集和沉积,加剧淀粉样斑块形成[23]。
OLFM3广泛存在于大脑和神经系统等组织器官中,在细胞发育迁移过程中刺激细胞紧密相连和黏附,调节细胞骨架形成,介导免疫细胞活化、增殖和炎症反应等。OLFM3可抑制免疫细胞活化状态,减少炎症细胞增殖和炎症介质产生[26], 调控神经元间相互作用,促进神经元迁移、突触形成及神经回路发育,进而促进神经系统正常发育[6]。动物实验[27]表明, 敲除癫痫小鼠模型OLFM3表达可影响AMPAR复合物形成,干扰小鼠学习、认知和运动功能。本研究发现, OLFM3表达下调参与AD的发生与发展。OLFM3表达降低影响神经元间黏附作用,导致神经元功能受损和信号传导紊乱,同时也影响突触形成和突触传递,导致记忆和认知功能下降[6]; AD患者炎症反应导致疾病不断恶化,机体为拮抗炎症反应不断消耗OLFM3,也可能导致其水平下降[7]。
本研究发现,脑脊液CTHRC1和OLFM3可作为诊断AD的标志物,并且联合检测诊断价值更高, AUC可达0.923。既往研究[28-29]证实,脑内老年斑及神经元纤维缠结是AD发病的主要机制。脑脊液Aβ-42、T-tau、P-tau等生物学指标与上述病理学改变密切相关, Aβ-42形成β样淀粉斑块可致神经元毒性,损害神经元结构和功能,导致神经元凋亡, T-tau及P-tau可影响神经元突触传递,导致神经元功能障碍和神经元网络受损,并与Aβ斑块形成及沉积有关。本研究发现,脑脊液CTHRC1和OLFM3与上述标志物相关,进一步说明脑脊液CTHRC1和OLFM3可能通过影响Aβ斑块沉积和介导神经元功能损伤参与AD发生与发展。本研究还发现,血清CTHRC1和OLFM3与AD患者认知功能障碍相关, CTHRC1升高可加剧神经炎症,并影响神经元间连接的强度和稳定性,导致大脑学习和记忆功能障碍,而OLFM3降低会导致神经营养因子减少,神经元正常发育受阻,氧化应激增强,导致细胞内氧化还原失衡,造成神经元受损。该结果同时表明,临床通过检测CTHRC1、OLFM3水平,可辅助评估AD病情严重程度,进而指导临床制订精准治疗方案,以改善患者预后。但本研究未分析CTHRC1、OLFM3在血液中的动态变化,未来还需探讨其在AD患者血液中的临床意义。同时,本研究病例来源于单一中心且样本量相对较小,可能限制研究结果的外推性,未来需扩大样本量、开展多中心的前瞻性队列研究,进一步检验结果的可靠性。
综上所述,血清CTHRC1表达上调和OLFM3表达下降介导了AD的发病过程,并与病情严重程度相关。早期CTHRC1、OLFM3联合检测可辅助临床诊断AD以及评估患者认知功能受损程度。
-
表 1 2组患者脑脊液的CTHRC1、OLFM3水平及脑脊液标志物(x±s)
指标 AD组(n=96) 对照组(n=60) t P CTHRC1/(μg/L) 35.02±5.89 27.67±5.14 7.952 < 0.001 OLFM3/(μg/mL) 12.64±2.89 17.15±3.37 8.895 < 0.001 Aβ-40/(pg/mL) 7 265.89±1 622.70 6 826.40±1 357.51 1.753 0.082 Aβ-42/(pg/mL) 304.78±114.05 467.16±135.83 8.034 < 0.001 Aβ-42/Aβ-40 0.04±0.02 0.09±0.02 15.192 < 0.001 T-tau/(pg/mL) 513.75±122.38 159.75±103.43 18.634 < 0.001 P-tau/(pg/mL) 79.56±22.64 51.02±17.92 8.279 < 0.001 CTHRC1: 胶原三螺旋重复蛋白-1; OLFM3: 溴素结构域家族蛋白3; Aβ-40: β-淀粉样蛋白-40;
Aβ-42: β-淀粉样蛋白-42; T-tau: 总tau蛋白; P-tau: 磷酸化tau蛋白。表 2 脑脊液CTHRC1、OLFM3对AD患者的诊断价值
指标 AUC 标准误 P 截断值 灵敏度 特异度 CTHRC1 0.839 0.036 < 0.001 32.18 μg/L 0.83 0.62 OLFM3 0.822 0.038 < 0.001 15.02 μg/mL 0.81 0.61 指标联合 0.923 0.021 < 0.001 — 0.95 0.77 表 3 不同病情严重程度AD患者的脑脊液CTHRC1、OLFM3及脑脊液标志物水平(x±s)
指标 轻度组(n=34) 中度组(n=39) 重度组(n=23) F P CTHRC1/(μg/L) 27.91±6.11 32.64±6.89* 49.57±7.30*# 75.235 < 0.001 OLFM3/(μg/mL) 15.81±3.04 11.58±2.79* 9.76±2.51*# 36.241 < 0.001 Aβ-40/(pg/mL) 7 231.38±1 595.10 7 268.25±1 620.07 7 312.91±1 613.34 0.018 0.982 Aβ-42/(pg/mL) 356.91±70.76 295.32±65.82* 243.76±61.92*# 20.379 < 0.001 Aβ-42/Aβ-40 0.06±0.02 0.03±0.01* 0.02±0.01*# 63.935 < 0.001 T-tau/(pg/mL) 460.89±86.97 519.23±93.41* 582.61±97.29*# 12.089 < 0.001 P-tau/(pg/mL) 67.77±20.43 80.13±22.38* 96.02±23.91*# 11.240 < 0.001 与轻度组比较, *P < 0.05; 与中度组比较, #P < 0.05。 表 4 不同病情严重程度AD患者的MMSE、MoCA评分(x±s)分
指标 轻度组(n=34) 中度组(n=39) 重度组(n=23) F P MMSE评分 25.34±5.02 21.03±4.87* 16.39±4.26*# 24.214 < 0.001 MoCA评分 25.59±4.68 21.72±4.13* 15.45±3.89*# 38.528 < 0.001 与轻度组比较, *P < 0.05; 与中度组比较, #P < 0.05。 表 5 AD患者脑脊液CTHRC1、OLFM3水平与病情严重程度及脑脊液标志物的关系
指标 CTHRC1 OLFM3 r或rs(95%CI) P r或rs(95%CI) P 病情严重程度 0.596(0.533~0.652) 0.001 -0.576(-0.627~-0.509) 0.003 Aβ-40 0.153(0.076~0.261) 0.349 0.229(0.101~0.375) 0.627 Aβ-42 -0.615(-0.661~-0.572) < 0.001 0.594(0.138~0.282) < 0.001 Aβ-42/Aβ-40 -0.639(-0.690~-0.594) < 0.001 0.601(0.568~0.654) < 0.001 T-tau 0.560(0.517~0.618) 0.003 -0.532(-0.579~-0.498) 0.005 P-tau 0.593(0.538~0.649) 0.002 -0.540(-0.591~-0.503) 0.004 MMSE评分 -0.627(-0.695~-0.572) < 0.001 0.597(0.534~0.649) < 0.001 MoCA评分 -0.641(-0.702~-0.599) < 0.001 0.611(0.568~0.673) 0.001 -
[1] SCHELTENS P, DE STROOPER B, KIVIPELTO M, et al. Alzheimer's disease[J]. Lancet, 2021, 397(10284): 1577-1590. doi: 10.1016/S0140-6736(20)32205-4
[2] KHAN S, BARVE K H, KUMAR M S. Recent advancements in pathogenesis, diagnostics and treatment of Alzheimer's disease[J]. Curr Neuropharmacol, 2020, 18(11): 1106-1125. doi: 10.2174/1570159X18666200528142429
[3] OGBODO J O, AGBO C P, NJOKU U O, et al. Alzheimer's disease: pathogenesis and therapeutic interventions[J]. Curr Aging Sci, 2022, 15(1): 2-25. doi: 10.2174/1874609814666210302085232
[4] RUIZ-VILLALBA A, ROMERO J P, HERNÁNDEZ S C, et al. Single-cell RNA sequencing analysis reveals a crucial role for CTHRC1 (collagen triple Helix repeat containing 1) cardiac fibroblasts after myocardial infarction[J]. Circulation, 2020, 142(19): 1831-1847. doi: 10.1161/CIRCULATIONAHA.119.044557
[5] WANG D, ZHANG Y P, YE T B, et al. Cthrc1 deficiency aggravates wound healing and promotes cardiac rupture after myocardial infarction via non-canonical WNT5A signaling pathway[J]. Int J Biol Sci, 2023, 19(4): 1299-1315. doi: 10.7150/ijbs.79260
[6] WANG H, DEY K K, CHEN P C, et al. Integrated analysis of ultra-deep proteomes in cortex, cerebrospinal fluid and serum reveals a mitochondrial signature in Alzheimer's disease[J]. Mol Neurodegener, 2020, 15(1): 43. doi: 10.1186/s13024-020-00384-6
[7] TANG S R, WANG T C, ZHANG X G, et al. Olfactomedin-3 enhances seizure activity by interacting with AMPA receptors in epilepsy models[J]. Front Cell Dev Biol, 2020, 8: 722. doi: 10.3389/fcell.2020.00722
[8] 中国痴呆与认知障碍写作组, 中国医师协会神经内科医师分会认知障碍疾病专业委员会. 2018中国痴呆与认知障碍诊治指南(二): 阿尔茨海默病诊治指南[J]. 中华医学杂志, 2018, 98(13): 971-977. [9] NOSHENY R L, YEN D, HOWELL T, et al. Evaluation of the electronic clinical dementia rating for dementia screening[J]. JAMA Netw Open, 2023, 6(9): e2333786.
[10] CAI S J, LI Z Q, WANG J, et al. Excessive daytime sleepiness in young and middle-aged Chinese adults with obstructive sleep apnea: implications for cognitive dysfunction[J]. Sleep Breath, 2024, 28(1): 113-121. doi: 10.1007/s11325-023-02854-9
[11] LIMA PEREIRA V, FREITAS S, SIMÕES M R, et al. Montreal Cognitive Assessment (MoCA): a validation study among prisoners[J]. Crim Behav Ment Health, 2023, 33(5): 330-341. doi: 10.1002/cbm.2306
[12] JIA L F, DU Y F, CHU L, et al. Prevalence, risk factors, and management of dementia and mild cognitive impairment in adults aged 60 years or older in China: a cross-sectional study[J]. Lancet Public Health, 2020, 5(12): e661-e671. doi: 10.1016/S2468-2667(20)30185-7
[13] JIA J P, WEI C B, CHEN S Q, et al. The cost of Alzheimer's disease in China and re-estimation of costs worldwide[J]. Alzheimers Dement, 2018, 14(4): 483-491. doi: 10.1016/j.jalz.2017.12.006
[14] 李冬梅. 经颅磁刺激联合药物治疗阿尔茨海默病改善患者认知功能、精神行为症状及神经递质的效果[J]. 中国临床医生杂志, 2023, 51(10): 1183-1185. [15] 张鑫, 王军燕, 魏玉婷, 等. 冈田酸诱导阿尔兹海默病动物模型的研究进展[J]. 实用临床医药杂志, 2022, 26(19): 129-134. doi: 10.7619/jcmp.20221475 [16] JUCKER M, WALKER L C. Alzheimer's disease: from immunotherapy to immunoprevention[J]. Cell, 2023, 186(20): 4260-4270. doi: 10.1016/j.cell.2023.08.021
[17] BREIJYEH Z, KARAMAN R. Comprehensive review on Alzheimer's disease: causes and treatment[J]. Molecules, 2020, 25(24): 5789. doi: 10.3390/molecules25245789
[18] 艾力克木·艾尔肯, 全贞贞, 庆宏. 阿尔茨海默症生物标志物在脑脊液和血液中的研究[J]. 生命科学, 2021, 33(8): 939-945. [19] 李小雄, 李金平, 黄洁, 等. 胰岛淀粉样多肽治疗阿尔茨海默病小鼠的circRNA和mRNA表达谱分析[J]. 中华全科医学, 2023, 21(7): 1101-1104. [20] 剌梅, 白雅红, 孙继红, 等. ABCA1基因多态性与阿尔茨海默病相关神经丝蛋白的关系[J]. 检验医学与临床, 2023, 20(7): 964-968. [21] MYNGBAY A, MANARBEK L, LUDBROOK S, et al. The role of collagen triple Helix repeat-containing 1 protein (CTHRC1) in rheumatoid arthritis[J]. Int J Mol Sci, 2021, 22(5): 2426. doi: 10.3390/ijms22052426
[22] BAI B, WANG X S, LI Y X, et al. Deep multilayer brain proteomics identifies molecular networks in Alzheimer's disease progression[J]. Neuron, 2020, 106(4): 700. doi: 10.1016/j.neuron.2020.04.031
[23] 陈俊, 郑锦豪, 陈家良, 等. 阿尔茨海默病患者血清GGT、CTHRC1表达水平检测及临床意义[J]. 天津医药, 2023, 51(2): 216-220. [24] FENG Y, HU J P, LIU F, et al. Collagen triple Helix repeat containing 1 deficiency protects against airway remodeling and inflammation in asthma models in vivo and in vitro[J]. Inflammation, 2023, 46(3): 925-940. doi: 10.1007/s10753-022-01781-3
[25] PLASCENCIA-VILLA G, PERRY G. Preventive and therapeutic strategies in Alzheimer's disease: focus on oxidative stress, redox metals, and ferroptosis[J]. Antioxid Redox Signal, 2021, 34(8): 591-610. doi: 10.1089/ars.2020.8134
[26] LEE C J, LEE H Y, YU Y S, et al. Brain compartmentalization based on transcriptome analyses and its gene expression in Octopus minor[J]. Brain Struct Funct, 2023, 228(5): 1283-1294. doi: 10.1007/s00429-023-02647-6
[27] SULTANA A, NAKAYA N, DONG L J, et al. Deletion of olfactomedin 2 induces changes in the AMPA receptor complex and impairs visual, olfactory, and motor functions in mice[J]. Exp Neurol, 2014, 261: 802-811. doi: 10.1016/j.expneurol.2014.09.002
[28] MILÀ-ALOMÀ M, SALVADÓ G, GISPERT J D, et al. Amyloid beta, tau, synaptic, neurodegeneration, and glial biomarkers in the preclinical stage of the Alzheimer's continuum[J]. Alzheimers Dement, 2020, 16(10): 1358-1371. doi: 10.1002/alz.12131
[29] XU Y N, JIANG H L, ZHU B, et al. Advances and applications of fluids biomarkers in diagnosis and therapeutic targets of Alzheimer's disease[J]. CNS Neurosci Ther, 2023, 29(8): 2060-2073. doi: 10.1111/cns.14238




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
