Effects of different treatment regimens on severe community-acquired pneumonia in children with a history of recurrent respiratory infections
-
摘要:目的
比较万古霉素、利奈唑胺单用及分别联合脾多肽治疗合并反复呼吸道感染史的重症儿童社区获得性肺炎(CAP)的临床效果。
方法选取296例合并反复呼吸道感染史的重症CAP患儿作为研究对象,采用随机数字表法分为万古霉素组(单用万古霉素)、利奈唑胺组(单用利奈唑胺)、联合A组(万古霉素联合脾多肽)、联合B组(利奈唑胺联合脾多肽),每组74例。比较4组患儿的疗效、康复进程(体温恢复正常时间、咳嗽好转时间、呼吸改善时间、住院时间)、不良反应发生情况、直接医疗成本,并通过决策树模型与成效比分析比较各组治疗方案的经济性。
结果利奈唑胺组、联合A组、联合B组治疗总有效率分别为83.78%、86.49%、97.30%, 均高于万古霉素组的71.62%, 且联合B组高于利奈唑胺组、联合A组,差异有统计学意义(P < 0.05)。利奈唑胺组、联合A组、联合B组体温恢复正常时间、呼吸改善时间、咳嗽好转时间、住院时间均短于万古霉素组,且联合B组均短于利奈唑胺组、联合A组,差异有统计学意义(P < 0.05)。4组患儿不良反应发生情况比较,差异无统计学意义(P>0.05)。4组患儿治疗成本、检查/检验成本、住院成本比较,差异无统计学意义(P>0.05); 利奈唑胺组、联合B组、万古霉素组、联合A组药品成本、总成本依次升高,两两比较差异有统计学意义(P < 0.05)。成效比从高至低依次为联合A组(75.84)、万古霉素组(73.22)、利奈唑胺组(32.87)、联合B组(32.69), 敏感性分析显示该成效比分析结果稳定可靠。
结论4种治疗方案中,利奈唑胺联合脾多肽对合并反复呼吸道感染史的重症CAP患儿的疗效最佳,患儿临床获益最明显,且成本-效果优势显著。
Abstract:ObjectiveTo compare the clinical effects of vancomycin, linezolid alone, and their separate combination with spleen polypeptide in the treatment of severe community-acquired pneumonia (CAP) in children with a history of recurrent respiratory infections.
MethodsA total of 296 children with severe CAP and a history of recurrent respiratory infections were selected as study subjects and randomly divided into four groups: vancomycin group (vancomycin alone), linezolid group (linezolid alone), combined group A (vancomycin combined with spleen polypeptide), and combined group B (linezolid combined with spleen polypeptide), with 74 patients in each group. The curative effects, recovery process (time to normalization of body temperature, time to improvement of cough, time to improvement of respiration, length of hospital stay), adverse reactions, and direct medical costs were compared among the four groups. Decision tree models and cost-effectiveness analysis were used to compare the economics of each treatment plan.
ResultsThe total effective rates in the linezolid group, combined group A, and combined group B were 83.78%, 86.49%, and 97.30%, respectively, which were all higher than 71.62% in the vancomycin group, and the combined group B had a higher effective rate than the linezolid group and combined group A (P < 0.05). The time to normalization of body temperature, improvement of respiration, improvement of cough, and length of hospital stay were shorter in the linezolid group, combined group A, and combined group B than in the vancomycin group, and were shorter in the combined group B compared to the linezolid group and combined group A (P < 0.05). There was no statistically significant difference in the occurrence of adverse reactions among the four groups (P>0.05). There were no statistically significant differences in treatment costs, examination/testing costs, and hospitalization costs among the four groups (P>0.05). The treatment costs and total costs were higher in the vancomycin group, combined group A, linezolid group, and combined group B in ascending order, with statistically significant between-group difference (P < 0.05). The cost-effectiveness ratios from high to low were combined group A (75.84), vancomycin group (73.22), linezolid group (32.87), and combined group B (32.69). Sensitivity analysis showed that the cost-effectiveness ratio analysis results were stable and reliable.
ConclusionAmong the four treatment options, the combination of linezolid and spleen polypeptide has the best therapeutic effect in severe CAP children with a history of recurrent respiratory infections, with the most significant clinical benefit and cost-effectiveness advantages.
-
儿童社区获得性肺炎(CAP)为肺实质和(或)肺间质组织的急性感染,病原菌以革兰阳性菌最为常见,患儿常表现为发热、呼吸困难、咳嗽、管状呼吸音等症状[1]。近年来,病原菌耐药问题日益突出,合并反复呼吸道感染史的重症患儿甲氧西林耐药情况增多, CAP治疗难度增大[2]。利奈唑胺、万古霉素是抗甲氧西林耐药菌的主要药物,但因儿童免疫功能较低,部分患儿可能久治不愈,加重了家庭及社会的医疗经济负担[3]。脾多肽作为免疫刺激剂,可增强机体免疫调节能力,提升疗效[4]。本研究以296例合并反复呼吸道感染史的重症CAP患儿为研究对象,基于疗效和经济学价值综合分析不同方案的价值,以期筛选出疗效好、成本低的治疗方案。
1. 对象与方法
1.1 研究对象
前瞻性选取2019年12月—2023年9月河北省儿童医院收治的合并反复呼吸道感染史的296例重症CAP患儿作为研究对象。纳入标准: ①有发热、咳嗽、肺部湿啰音、呼吸困难等临床症状或体征,X线检查可见阴影弥漫,且符合重症CAP诊断标准[5]者; ②合并反复呼吸道感染史,符合《儿童反复上呼吸道感染临床诊治管理专家共识》[6]中相关诊断标准者; ③入院时体液/细胞免疫指标存在≥1项异常者; ④痰标本耐药菌试验显示耐甲氧西林革兰阳性菌者; ⑤家属知晓研究方案风险及获益,承诺配合研究,自愿签署同意书者。排除标准: ①首次感染入院者; ②细菌感染病原菌不明者; ③入院时已出现心力衰竭等严重并发症者; ④对研究药物过敏者; ⑤伴有先天性凝血或免疫疾病者; ⑥合并严重全身性感染者; ⑦合并心、肝、肾等重要器官功能障碍者; ⑧合并先天性呼吸道器官发育不全者; ⑨合并支气管畸形或异常者; ⑩合并哮喘者。采用SPSS 23.0软件以随机数字表法将患儿分别纳入万古霉素组、利奈唑胺组、联合A组、联合B组,每组74例。本研究经河北省儿童医院伦理委员会审核批准[院科伦审: (2019)伦审第(1137)号]。
1.2 方法
各组患儿治疗前肾功能指标、血小板计数均处于正常范围内,接受常规综合治疗,包括祛痰、镇静、平喘、营养支持、吸氧、抗革兰阴性菌感染、维持出入量平衡等,定期(治疗3、7、10 d)记录患儿体温、血小板计数、白细胞计数、病原菌培养结果和影像学检查结果等。病原菌培养结果未出前,所有患儿接受相同的广谱经验性抗感染治疗。严格消毒口腔后留取痰液,病原菌培养及耐药性检测结果提示患儿病原菌均为耐甲氧西林革兰阳性菌。
① 万古霉素组: 给予万古霉素(浙江医药股份有限公司新昌制药厂,国药准字H20033366, 规格0.5 g/瓶)静脉注射治疗,每次15 mg/kg, 每8 h给药1次,连续给药7~10 d。②利奈唑胺组: 给予利奈唑胺(Fresenius Kabi Norge AS, 批准文号HJ20160301, 规格为300 mL含利奈唑胺0.6 g与葡萄糖15.0 g)静脉注射治疗,每次10 mg/kg, 每8 h给药1次,连续给药7~14 d。③联合A组: 给予万古霉素(用法同万古霉素组,连续给药7~14 d)联合脾多肽(融致丰生制药有限公司,国药准字H22026497, 规格2 mL/支)治疗,参照文献[7]确定脾多肽剂量与给药方式(肌注治疗),每次2~4 mL, 1次/d, 连续给药7~10 d。④联合B组: 给予利奈唑胺(用法同利奈唑胺组)联合脾多肽(用法同联合A组)治疗,连续用药7~14 d。
1.3 观察指标
① 疗效: 参照文献[6], 于治疗14 d后对各组患儿进行疗效评估(以患儿临床症状、胸部X线检查结果和实验室检查结果为依据)。痊愈是指治疗14 d后患儿发热、呼吸困难等症状完全消失,胸部X线检查、实验室检查结果均正常; 显效是指患儿临床症状明显好转,检查结果基本恢复正常; 好转是指患儿临床症状好转,检查结果显示病情减轻; 无效是指患儿临床症状未好转,检查结果无变化甚至加重。总有效率=(痊愈+显效)/总例数×100%。②康复进程: 统计各组患儿咳嗽好转时间、体温恢复正常时间、呼吸改善时间和住院时间。③不良反应: 统计各组患儿治疗期间腹泻、肾损伤、血小板减少、恶心或呕吐等不良反应发生情况。④直接医疗成本: 于患儿病情康复后统计医疗成本(易于统计的直接医疗成本),包括药品成本、治疗成本、检查/检验成本、住院成本,各项合计为总成本。⑤决策树模型[10]: 以各组治疗方案为决策点,以相应治疗效果(总有效、无效)及费用为决策分支,构建决策树模型。⑥成效比分析: 总成本=痊愈率×痊愈成本+显效率×显效成本+好转率×好转成本+无效率×无效成本。成效比越低提示药物经济学优势越大。
1.4 统计学分析
采用SPSS 22.0统计学软件分析数据,建立EXCEL数据库进行常规逻辑检错。符合正态分布的计量资料以(x±s)表示,组内比较行配对样本t检验,组间比较行独立样本t检验。计数资料以[n(%)]表示,行χ2检验(若理论频数 < 1,采用Fisher's精确概率法,若理论频数为1~5, 采用校正检验)。P < 0.05为差异有统计学意义。
2. 结果
2.1 一般资料
4组患儿性别、年龄、病程、体质量、主要照顾者文化程度比较,差异无统计学意义(P>0.05), 见表 1。
表 1 各组患儿一般资料比较(x±s)[n(%)]指标 分类 万古霉素组(n=74) 利奈唑胺组(n=74) 联合A组(n=74) 联合B组(n=74) 性别 男 33(44.59) 27(36.49) 30(40.54) 29(39.19) 女 41(55.41) 47(63.51) 44(59.46) 45(60.81) 年龄/岁 6.01±1.71 5.77±1.84 6.34±2.01 6.27±1.69 病程/d 5.01±1.24 4.87±0.98 4.82±0.96 5.06±1.33 体质量/kg 20.37±2.26 20.87±2.39 21.03±2.79 20.45±2.55 主要照顾者文化程度 大专及以上 28(37.84) 30(40.54) 28(37.84) 31(41.89) 中专或高中 31(41.89) 30(40.54) 29(39.19) 30(40.54) 初中及以下 15(20.27) 14(18.92) 17(22.97) 13(17.57) 2.2 疗效
利奈唑胺组、联合A组、联合B组治疗总有效率均高于万古霉素组,联合B组治疗总有效率高于利奈唑胺组、联合A组,差异有统计学意义(P < 0.05); 联合A组治疗总有效率与利奈唑胺组比较,差异无统计学意义(P>0.05), 见表 2。
表 2 各组患儿疗效比较[n(%)]组别 n 痊愈 显效 好转 无效 总有效 万古霉素组 74 20(27.03) 33(44.59) 12(16.22) 9(12.16) 53(71.62) 利奈唑胺组 74 41(55.41) 21(28.38) 8(10.81) 4(5.41) 62(83.78)*# 联合A组 74 42(56.76) 22(29.73) 7(9.46) 3(4.05) 64(86.49)*# 联合B组 74 59(79.73) 13(17.57) 2(2.70) 0 72(97.30)* 与万古霉素组比较, * P < 0.05; 与联合B组比较, #P < 0.05。 2.3 康复进程
利奈唑胺组、联合A组、联合B组体温恢复正常时间、呼吸改善时间、咳嗽好转时间、住院时间均短于万古霉素组,且联合B组均短于利奈唑胺组、联合A组,差异有统计学意义(P < 0.05); 联合A组体温恢复正常时间、呼吸改善时间、咳嗽好转时间、住院时间与利奈唑胺组比较,差异无统计学意义(P>0.05), 见表 3。
表 3 各组患儿康复进程比较(x±s)d 组别 n 体温恢复正常时间 呼吸改善时间 咳嗽好转时间 住院时间 万古霉素组 74 7.84±2.57 8.76±2.80 11.12±3.59 21.44±4.09 利奈唑胺组 74 6.12±2.01*# 7.05±2.31*# 9.58±3.17*# 18.03±3.67*# 联合A组 74 5.94±1.83*# 6.82±2.24*# 9.47±3.13*# 17.54±4.32*# 联合B组 74 4.68±1.50* 5.30±1.65* 7.03±2.25* 13.86±4.20* 与万古霉素组比较, * P < 0.05; 与联合B组比较,#P < 0.05。 2.4 不良反应
4组患儿不良反应发生情况比较,差异无统计学意义(P>0.05), 见表 4。
表 4 各组患儿不良反应发生情况比较[n(%)]组别 n 腹泻 恶心或呕吐 肾损伤 血小板减少 万古霉素组 74 3(4.05) 2(2.70) 0 0 利奈唑胺组 74 1(1.35) 3(4.05) 1(1.35) 1(1.35) 联合A组 74 2(2.70) 1(1.35) 1(1.35) 0 联合B组 74 3(4.05) 2(2.70) 1(1.35) 1(1.35) 2.5 直接医疗成本
各组患儿治疗成本、检查/检验成本、住院成本比较,差异无统计学意义(P>0.05); 利奈唑胺组、联合B组、万古霉素组、联合A组药品成本、总成本依次升高,两两比较差异有统计学意义(P < 0.05), 见表 5。
表 5 各组患儿直接医疗成本比较(x±s)元人民币 组别 n 药品成本 治疗成本 检查/检验成本 住院成本 总成本 万古霉素组 74 4 459.10±682.15 176.40±20.31 257.58±61.99 351.25±98.03 5 244.33±864.79 利奈唑胺组 74 1 968.12±700.96* 177.53±18.64 261.73±76.52 346.77±94.58 2 754.15±718.33* 联合A组 74 5 778.98±696.83*# 180.95±24.76 259.00±68.45 340.59±82.66 6 559.52±850.06*# 联合B组 74 2 406.13±707.27*#△ 174.79±22.52 260.92±73.00 338.89±91.27 3 180.73±743.28*#△ 与万古霉素组比较, * P < 0.05; 与利奈唑胺组比较, #P < 0.05; 与联合A组比较, △P < 0.05。 2.6 决策树模型
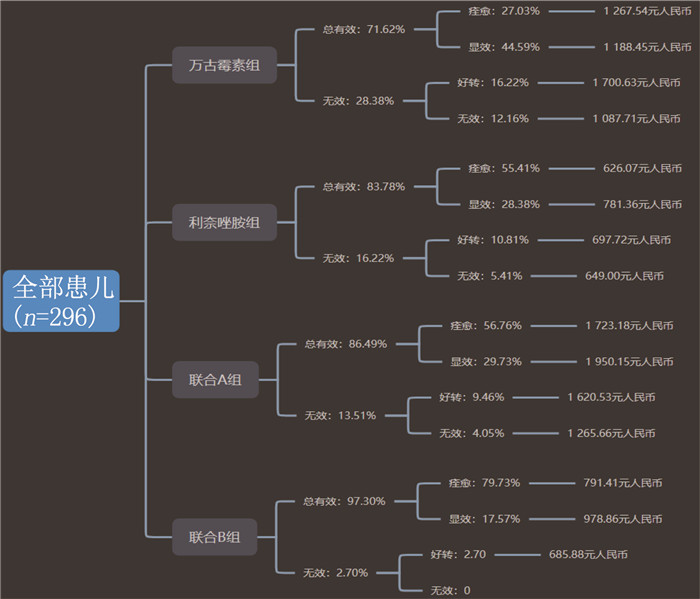
将不同治疗方案作为决策点,将不同治疗方案的效果及费用情况作为决策分支,应用Tree Age Pro软件构建决策树模型,见图 1。
2.7 成效比分析
以治疗总有效率为效果,万古霉素组取得每个单位效果的成本为73.22元人民币,利奈唑胺组为32.87元人民币,联合A组为75.84元人民币,联合B组为32.69元人民币,即取得每个单位效果的成本排序结果为联合A组>万古霉素组>利奈唑胺组>联合B组; 每增加1个单位效果,联合A组、万古霉素组、利奈唑胺组分别比联合B组多付出312.56、80.36、31.55元人民币。为检查成效比分析结果的稳定性,本研究将成本下降10%进行敏感性分析,结果显示,联合A组、万古霉素组、利奈唑胺组取得单位效果所需成本仍高于联合B组,说明成效比分析结果稳定可靠,见表 6。
表 6 各组患儿成效比分析结果分析类别 组别 成本/元人民币 效果/% 成效比 成效比变化值 成效比分析 万古霉素组 5 244.33 71.62 73.22 80.36 利奈唑胺组 2 754.15 83.78 32.87 31.55 联合A组 6 559.52 86.49 75.84 312.56 联合B组 3 180.73 97.30 32.69 — 敏感性分析 万古霉素组 4 719.90 71.62 65.90 72.32 利奈唑胺组 2 478.74 83.78 29.59 28.40 联合A组 5 903.57 86.49 68.26 281.31 联合B组 2 862.66 97.30 29.42 — 3. 讨论
本研究结果显示,利奈唑胺组治疗总有效率和康复进程均显著优于万古霉素组(P < 0.05), 提示单用利奈唑胺的治疗效果优于单用万古霉素,与房东东等[9]研究结果相似。万古霉素是治疗革兰阳性球菌感染的常用糖肽类抗生素,其作用机制是通过干扰细菌细胞壁合成抑制病菌繁殖以抗感染,该药最低抑菌浓度随葡萄球菌数目增加而升高,但存在一定肾毒性,不适用于肾损伤患者[10]。随着耐万古霉素肠球菌数目的增加,万古霉素的抗菌效果降低[11]。MVHLBERG E等[12]提出可通过对万古霉素进行结构修饰解决多重耐药性问题,但有待长期实践加以证实。目前,利奈唑胺已被批准用于治疗万古霉素耐药金黄色葡萄球菌感染等[13]。FU X Y等[14]报道,万古霉素最低抑菌浓度>1 g/mL时,宜选用利奈唑胺作为替代治疗药物。利奈唑胺是新型噁唑烷酮类抗生素,不受细菌对50S核糖体亚单位抗菌药物耐药性的影响,不易出现交叉耐药情况,抗菌作用显著[15]。KATO H等[16]指出,利奈唑胺治疗耐甲氧西林金黄色葡萄球菌肺炎的效果较好。利奈唑胺的组织、体液渗透性好,在皮肤、肺部、肌肉等组织中均能达到较好浓度,可充分发挥抗菌作用,提升疗效[17]。
刘峰等[18]指出,联用脾多肽可提升老年重症肺部感染患者的临床疗效,缓解临床症状,促进病情恢复。本研究亦发现,联用脾多肽可提升治疗效果,这与脾多肽能增强机体免疫调节功能相关。脾多肽是新型免疫刺激剂,已被广泛用于癌症化疗患者的辅助治疗中,可提高癌症患者T淋巴细胞亚群水平,改善机体免疫功能[19]。作为辅助治疗药物,脾多肽能通过增强免疫细胞表面抗原活性,提高淋巴细胞免疫功能,增强机体抗感染能力[20]。相关研究[19]发现,将脾多肽应用于重症呼吸机相关性肺炎的治疗中,可显著缩短抗菌药物使用时间,提升抗菌效果,提示脾多肽可作为重症感染患者的辅助治疗药物。本研究结果显示,联合B组的治疗总有效率最高,联合A组、利奈唑胺组次之,万古霉素组最低,提示利奈唑胺联合脾多肽治疗重症儿童CAP的效果可靠。本研究还发现, 4组患儿不良反应发生情况差异无统计学意义(P>0.05), 说明利奈唑胺与脾多肽联合治疗的安全性高。
本研究基于经济学角度对不同方案的检查/检验成本、药品成本等直接医疗成本进行分析发现,联合A组、联合B组的药品成本、总成本分别显著高于万古霉素组、利奈唑胺组(P < 0.05)。医疗成本、疗效均为选择治疗方案的重要考虑因素,因此,本研究进一步绘制决策树模型,并对4种治疗方案进行成效比分析。决策树模型作为一种动态分析模型,可评估方案风险及可行性,适用于治疗周期较短疾病的药物经济学分析。CAP治疗周期较短,1周内病情可得到有效控制,医生根据患儿病情变化合理调整用药方案,可采用决策树模型分析。成效比分析的目的是在确保疗效的基础上控制治疗成本,筛选最优方案。本研究结果显示,联合B组成效比最低,其次为利奈唑胺组、万古霉素组,联合A组最高。以联合B组作为参考,其余3组成效比变化值均为正数,提示成本降低,其疗效降低,故联合B组方案最具经济性。采用概率敏感性分析(成本费用±10%)对成效比分析结果进行验证,得出结果与基础结果一致,表明成效比分析结果较为稳健,可信度较高。本研究4组方案中,联合B组的治疗方案最具成效比优势,且治疗效果最优,提示临床治疗合并反复呼吸道感染史的重症CAP患儿时,可将脾多肽联合利奈唑胺作为首选治疗方案。
但本研究样本量偏少,且不同厂家药物的定价及效果存在差异,可能造成实验结果偏差,此外本研究未对患儿体液与细胞免疫功能进行随访观察,未来还需进一步开展大样本量长周期研究加以验证。
-
表 1 各组患儿一般资料比较(x±s)[n(%)]
指标 分类 万古霉素组(n=74) 利奈唑胺组(n=74) 联合A组(n=74) 联合B组(n=74) 性别 男 33(44.59) 27(36.49) 30(40.54) 29(39.19) 女 41(55.41) 47(63.51) 44(59.46) 45(60.81) 年龄/岁 6.01±1.71 5.77±1.84 6.34±2.01 6.27±1.69 病程/d 5.01±1.24 4.87±0.98 4.82±0.96 5.06±1.33 体质量/kg 20.37±2.26 20.87±2.39 21.03±2.79 20.45±2.55 主要照顾者文化程度 大专及以上 28(37.84) 30(40.54) 28(37.84) 31(41.89) 中专或高中 31(41.89) 30(40.54) 29(39.19) 30(40.54) 初中及以下 15(20.27) 14(18.92) 17(22.97) 13(17.57) 表 2 各组患儿疗效比较[n(%)]
组别 n 痊愈 显效 好转 无效 总有效 万古霉素组 74 20(27.03) 33(44.59) 12(16.22) 9(12.16) 53(71.62) 利奈唑胺组 74 41(55.41) 21(28.38) 8(10.81) 4(5.41) 62(83.78)*# 联合A组 74 42(56.76) 22(29.73) 7(9.46) 3(4.05) 64(86.49)*# 联合B组 74 59(79.73) 13(17.57) 2(2.70) 0 72(97.30)* 与万古霉素组比较, * P < 0.05; 与联合B组比较, #P < 0.05。 表 3 各组患儿康复进程比较(x±s)
d 组别 n 体温恢复正常时间 呼吸改善时间 咳嗽好转时间 住院时间 万古霉素组 74 7.84±2.57 8.76±2.80 11.12±3.59 21.44±4.09 利奈唑胺组 74 6.12±2.01*# 7.05±2.31*# 9.58±3.17*# 18.03±3.67*# 联合A组 74 5.94±1.83*# 6.82±2.24*# 9.47±3.13*# 17.54±4.32*# 联合B组 74 4.68±1.50* 5.30±1.65* 7.03±2.25* 13.86±4.20* 与万古霉素组比较, * P < 0.05; 与联合B组比较,#P < 0.05。 表 4 各组患儿不良反应发生情况比较[n(%)]
组别 n 腹泻 恶心或呕吐 肾损伤 血小板减少 万古霉素组 74 3(4.05) 2(2.70) 0 0 利奈唑胺组 74 1(1.35) 3(4.05) 1(1.35) 1(1.35) 联合A组 74 2(2.70) 1(1.35) 1(1.35) 0 联合B组 74 3(4.05) 2(2.70) 1(1.35) 1(1.35) 表 5 各组患儿直接医疗成本比较(x±s)
元人民币 组别 n 药品成本 治疗成本 检查/检验成本 住院成本 总成本 万古霉素组 74 4 459.10±682.15 176.40±20.31 257.58±61.99 351.25±98.03 5 244.33±864.79 利奈唑胺组 74 1 968.12±700.96* 177.53±18.64 261.73±76.52 346.77±94.58 2 754.15±718.33* 联合A组 74 5 778.98±696.83*# 180.95±24.76 259.00±68.45 340.59±82.66 6 559.52±850.06*# 联合B组 74 2 406.13±707.27*#△ 174.79±22.52 260.92±73.00 338.89±91.27 3 180.73±743.28*#△ 与万古霉素组比较, * P < 0.05; 与利奈唑胺组比较, #P < 0.05; 与联合A组比较, △P < 0.05。 表 6 各组患儿成效比分析结果
分析类别 组别 成本/元人民币 效果/% 成效比 成效比变化值 成效比分析 万古霉素组 5 244.33 71.62 73.22 80.36 利奈唑胺组 2 754.15 83.78 32.87 31.55 联合A组 6 559.52 86.49 75.84 312.56 联合B组 3 180.73 97.30 32.69 — 敏感性分析 万古霉素组 4 719.90 71.62 65.90 72.32 利奈唑胺组 2 478.74 83.78 29.59 28.40 联合A组 5 903.57 86.49 68.26 281.31 联合B组 2 862.66 97.30 29.42 — -
[1] SMITH D K, KUCKEL D P, RECIDORO A M. Community-acquired pneumonia in children: rapid evidence review[J]. Am Fam Physician, 2021, 104(6): 618-625.
[2] 王珊珊, 徐丽, 陈泽辉, 等. 金黄色葡萄球菌临床分布及耐药性分析的单中心研究[J]. 实用临床医药杂志, 2022, 26(19): 83-86, 91. doi: 10.7619/jcmp.20221457 [3] OHASHI T, FUJITA Y, IRISAWA H, et al. Clinical efficacy and safety of arbekacin against pneumonia in febrile neutropenia: a retrospective study in patients with hematologic malignancies[J]. Infect Chemother, 2022, 54(1): 80-90. doi: 10.3947/ic.2021.0126
[4] YAN W, YAN S Q, HE W. Clinical efficacy of laparoscopic billroth Ⅱ subtotal gastrectomy plus lienal polypeptide injection for gastric cancer[J]. Evid Based Complement Alternat Med, 2022, 2022: 5162225.
[5] BRADLEY J S, BYINGTON C L, SHAH S S, et al. The management of community-acquired pneumonia in infants and children older than 3 months of age: clinical practice guidelines by the Pediatric Infectious Diseases Society and the Infectious Diseases Society of America[J]. Clin Infect Dis, 2011, 53(7): e25-e76. doi: 10.1093/cid/cir531
[6] 中国医师协会儿科医师分会儿童耳鼻咽喉专业委员会. 儿童反复上呼吸道感染临床诊治管理专家共识[J]. 中国实用儿科杂志, 2017, 32(10): 721-725. https://www.cnki.com.cn/Article/CJFDTOTAL-ZSEK201710001.htm [7] 张燕芬. 2011-2021年江苏省137例脾多肽注射液不良反应分析[J]. 中国新药杂志, 2022, 31(12): 1236-1240. https://www.cnki.com.cn/Article/CJFDTOTAL-ZXYZ202212016.htm [8] LUO X D, WEN X H, ZHOU M C, et al. Decision-tree-initialized dendritic neuron model for fast and accurate data classification[J]. IEEE Trans Neural Netw Learn Syst, 2022, 33(9): 4173-4183. doi: 10.1109/TNNLS.2021.3055991
[9] 房东东, 杨逢永, 李学军, 等. ICU医院获得性MRSA肺炎患者的菌株耐药基因分析及利奈唑胺和万古霉素的治疗效果[J]. 广西医学, 2022, 44(12): 1323-1327. https://www.cnki.com.cn/Article/CJFDTOTAL-GYYX202212002.htm [10] FLINT A J, DAVIS A P. Vancomycin mimicry: towards new supramolecular antibiotics[J]. Org Biomol Chem, 2022, 20(39): 7694-7712. doi: 10.1039/D2OB01381A
[11] JOSHI S, SHALLAL A, ZERVOS M. Vancomycin-resistant enterococci: epidemiology, infection prevention, and control[J]. Infect Dis Clin North Am, 2021, 35(4): 953-968. doi: 10.1016/j.idc.2021.07.002
[12] MÜHLBERG E, UMSTÄTTER F, KLEIST C, et al. Renaissance of vancomycin: approaches for breaking antibiotic resistance in multidrug-resistant bacteria[J]. Can J Microbiol, 2020, 66(1): 11-16. doi: 10.1139/cjm-2019-0309
[13] QIN Y, ZHANG L L, YE Y R, et al. Parametric population pharmacokinetics of linezolid: a systematic review[J]. Br J Clin Pharmacol, 2022, 88(9): 4043-4066. doi: 10.1111/bcp.15368
[14] FU X Y, LIN Z Q, CHEN S M, et al. Treatment of intracranial infection caused by methicillin-resistant Staphylococcus epidermidis with linezolid following poor outcome of vancomycin therapy: a case report and literature review[J]. Infect Drug Resist, 2021, 14: 2533-2542. doi: 10.2147/IDR.S319013
[15] CONRADIE F, BAGDASARYAN T R, BORISOV S, et al. Bedaquiline-pretomanid-linezolid regimens for drug-resistant tuberculosis[J]. N Engl J Med, 2022, 387(9): 810-823. doi: 10.1056/NEJMoa2119430
[16] KATO H, HAGIHARA M, ASAI N, et al. Meta-analysis of vancomycin versus linezolid in pneumonia with proven methicillin-resistant Staphylococcus aureus[J]. J Glob Antimicrob Resist, 2021, 24: 98-105. doi: 10.1016/j.jgar.2020.12.009
[17] THWAITES G, NGUYEN N V. Linezolid for drug-resistant tuberculosis[J]. N Engl J Med, 2022, 387(9): 842-843. doi: 10.1056/NEJMe2208554
[18] 刘峰, 谭焰, 许尤玲, 等. 乙酰半胱氨酸雾化吸入联合脾多肽治疗老年重症肺部感染对血清游离促肾上腺皮质激素、皮质醇水平的影响[J]. 实用老年医学, 2022, 36(2): 154-157. https://www.cnki.com.cn/Article/CJFDTOTAL-SYLA202202012.htm [19] 闫睿, 赵敏, 韩冬. 脾多肽注射液联合替吉奥+顺铂方案治疗晚期胃癌的效果及对外周血γ干扰素/白细胞介素4比值、T淋巴细胞亚群水平的影响[J]. 广西医学, 2021, 43(13): 1547-1552. https://www.cnki.com.cn/Article/CJFDTOTAL-GYYX202113005.htm [20] 范小红, 孙丽华. 脾多肽联合PAD对多发性骨髓瘤血清BALP、β-CTX和OPG水平的影响[J]. 检验医学与临床, 2021, 18(18): 2683-2687. https://www.cnki.com.cn/Article/CJFDTOTAL-JYYL202118015.htm -
期刊类型引用(1)
1. 赵佳宝,张松林,王慧敏. 肺部超声联合血清指标对儿童社区获得性肺炎的临床诊断价值. 实用临床医药杂志. 2025(03): 104-107+113 .  本站查看
本站查看
其他类型引用(0)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号