Effect of coronary CT angiography in evaluation of in-stent restenosis based on intravascular ultrasound
-
摘要:目的
以血管内超声(IVUS)为"金标准", 评估冠状动脉CT血管造影(CCTA)对经皮冠状动脉介入治疗(PCI)术后支架内再狭窄(ISR)的检测准确性。
方法回顾性收集同时期(4周内)行CCTA和IVUS检查的PCI术后患者的基本资料和影像学资料, 共纳入60例患者的80处目标血管(血管内置入支架)。根据患者置入支架内径将纳入病变分为A组(内径>3.0 mm)和B组(内径≤3.0 mm), 并根据病变所在节段(支架内部或支架边缘5 mm内)将A组/B组分为A1组/B1组(支架内部病变)和A2组/B2组(边缘病变), A1组加B1组为1组, A2组加B2组为2组。以IVUS判读结果为"金标准", 评估CCTA对支架内病变的定量检测结果和对不同内径、不同节段ISR的诊断准确性。
结果CCTA对支架内病变的定量检测结果(最小管腔内径、平均血管内径、最小管腔面积、斑块面积、斑块长度、外弹力膜面积、斑块负荷和斑块体积)与IVUS定量检测结果呈显著正相关(P < 0.001)。CCTA识别A组(n=41) ISR的特异性(92.86%)、灵敏性(92.59%)、准确性(92.68%)均较高, 与IVUS结果一致性较好(Kappa=0.840, P < 0.001);CCTA识别B组(n=39) ISR的特异性(88.24%)、灵敏性(86.36%)、准确性(87.18%)低于A组, 与IVUS结果一致性一般(Kappa=0.741, P < 0.001)。CCTA对A组、B组的识别结果比较, 差异无统计学意义(P=0.523);CCTA对1组、2组的识别结果比较, 差异无统计学意义(P=0.212);CCTA对A2组、B2组的识别结果比较, 差异无统计学意义(P=0.484);CCTA对A1组、B1组的识别结果比较, 差异有统计学意义(P=0.011)。
结论CCTA对ISR的定量检测结果准确性较好, 识别内径>3.0 mm的支架内部ISR和不同内径支架边缘ISR的结果可信度较高, 但对内径≤3.0 mm的内部支架ISR的诊断结果不准确。
-
关键词:
- 冠心病 /
- 冠状动脉CT血管造影 /
- 血管内超声 /
- 支架内再狭窄 /
- 支架内径 /
- 经皮冠状动脉介入治疗
Abstract:ObjectiveTo explore the accuracy of coronary CT angiography (CCTA) in evaluation of postoperative in-stent restenosis (ISR) after percutaneous coronary intervention (PCI) taking intravascular ultrasound (IVUS) as golden criteria.
MethodsThe basic information and imaging data of 60 patients (80 target vessels with intravascular stents) with coronary stent implantation who underwent CCTA and IVUS within 4 weeks in the same period were retrospectively collected.According to the diameter of stents, target vessels were divided into group A (stent diameter>3.0 mm) and group B (stent diameter≤ 3.0 mm).Group A and group B were further divided into group A1 and group B1(internal stent lesion), and group A2 and group B2(edge lesion) according to the lesion segment (inside stent or within 5 mm of stent edge).Group 1 included group A1 and group B1, and group 2 included group A2 and group B2.The IVUS results were taken as "gold standard" to evaluate the results of CCTA in quantitative detection of in-stent lesions and its accuracy in diagnosing in-stent lesions with different inner diameters and in different ISR segments.
ResultsThe quantitative results of CCTA in in-stent lesions (minimum lumen diameter, mean vessel diameter, minimum lumen area, plaque area, plaque length, external elastic membrane area, plaque load and plaque volume) had significant positive correlations with the quantitative results of IVUS (P < 0.001).The specificity (92.86%), sensitivity (92.59%) and accuracy (92.68%) of ISR by CCTA in group A (n=41) were higher, and were consistent with the results of IVUS (Kappa=0.840, P < 0.001).The specificity (88.24%), sensitivity (86.36%) and accuracy (87.18%) of ISR by CCTA in the group B were lower than those of the group A, which had moderate consistence with the results of IVUS (Kappa=0.741, P < 0.001).There was no significant difference in the diagnosis of identifying ISR between group A and B (P=0.523), between group 1 and group 2(P=0.212) and between group A2 and group B2(P=0.484).However, there was significant difference in the diagnosis of identifying ISR between group A1 and B1 by CCTA (P=0.011).
ConclusionCCTA has good accuracy in quantitative detection of ISR, and has higher reliability in identification of ISR in in-stent with diameter >3.0 mm and at the edge of stents with different inner diameters, but the diagnosis of internal stent ISR with diameter ≤3.0 mm is inaccurate.
-
目前,经皮冠状动脉介入治疗(PCI)已成为冠心病(CAD)的主要治疗手段。支架内再狭窄(ISR)是PCI术后最常见的并发症。研究[1]显示,即便使用第2代药物涂层支架(DESs), 术后1年再狭窄率仍然达到5%~10%。无创检查能够准确地识别ISR, 对于改善CAD患者预后和减少主要不良心血管事件(MACE)发生具有重要意义[2]。冠状动脉CT血管造影(CCTA)诊断原发性冠状动脉病变具有较高的特异性和灵敏性,已被广泛应用于临床。但关于CCTA在支架内病变尤其是ISR评估中的应用效果,相关研究[3-4]结论尚存争议。血管内超声(IVUS)对原发性及支架置入术后冠状动脉病变具有较高的检测准确性,是诊断血管内病变的“金标准”[5]。本研究以同时期的IVUS检测结果为“金标准”,评估CCTA对PCI术后支架内不同节段病变的检测准确性,现报告如下。
1. 资料与方法
1.1 一般资料
连续选取2019年9月—2021年9月于徐州医科大学附属医院就诊的PCI术后患者作为研究对象。纳入标准: ①同时期(4周内)接受CCTA和IVUS检查,且2次检查期间病情无明显进展(心电图ST段改变、心肌酶升高以及新发或加重的胸痛症状[6])者; ② CCTA图像质量为优或良(无伪影或轻度伪影, 4分制Likert评分为3~4分[7])。排除标准: ① CCTA图像质量一般或差(有中度、重度伪影)者; ② CCTA和IVUS检查时间相隔4周以上者; ③ IVUS检查前已进行病变血管扩张治疗者。本回顾性研究经医院伦理委员会审核批准。
1.2 影像学检查方法
1.2.1 CCTA检查
患者的冠状动脉CT影像学资料均使用螺旋CT机(SOMATOM Definition, SIEMENS Germany)获得。将对比剂(60~80 mL碘海醇及50 mL生理盐水)于肘静脉推注,流速5 mL/s。6 s延迟后,使用对比剂追踪技术至升主动脉根部水平触发1次5~12 s的增强扫描。触发阈值为90~100 Hu, 扫描参数为管内电流280~350 mA、管内电压120 kV, 扫描区域为气管隆突下1.0 cm至心脏下缘1.5 cm。
1.2.2 IVUS检查
于冠状动脉造影(CAG)术后进行,使用美国Boston Scientific公司Opticross机械式超声导管,应用3.6F×135 cm的成像导丝,频率设定为40 MHz。将超声导管经冠状动脉导丝送至靶血管的远端,以0.5 mm/s速度匀速向冠状动脉口回撤,全程记录靶血管的二维切面影像。
1.3 图像处理及测量
1.3.1 CCTA
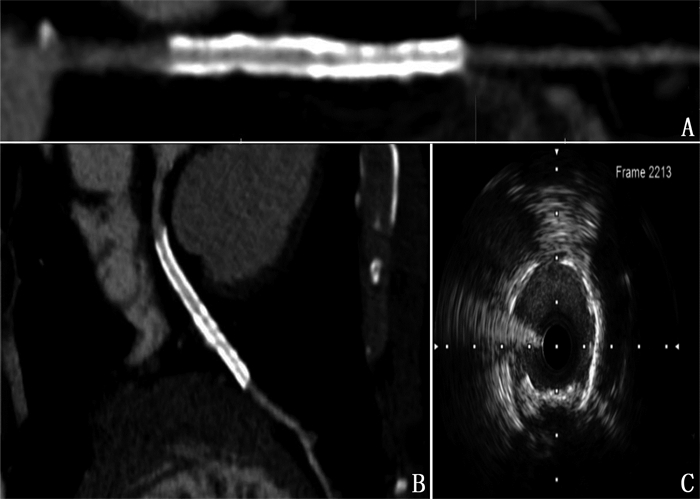
所得图像在Philips Intellispace Portal工作站后处理,运用多层面重建(MPR)、曲面重建(CPR)后处理技术,定位支架内或支架前后边缘5 mm内病变最重处(见图 1、图 2),对目标斑块进行定量检测,测量最小管腔内径(MLD)、病变前后正常血管内径(D1、D2)、最小管腔面积(MLA)、外弹力膜面积(EEMA)和斑块长度(PL), 计算斑块面积(PA, PA=EEMA-MLA)、斑块体积(PV, PV=PA×PL)和斑块负荷(PB, PB=MLA/EEMA)[8-9], 同时计算平均血管内径(MD)和狭窄率, MD=(D1+D2)/2, 狭窄率=(MD-MLD)/MD。ISR定义为支架内狭窄率>50%或支架前后5 mm血管内狭窄>50%[10]。CCTA的图像由2位心血管放射科医生回顾性评估,2位医生对冠状动脉造影和IVUS除上述定位标准外的结果均不知情,取二者定量检测的平均值用于进一步分析。
1.3.2 IVUS
运用Boston Scientific Image Viewer系统逐帧分析获取的超声图像,选取与CCTA同一目标处病变(见图 1、图 2),测量该斑块的起始部至冠状动脉口或解剖学标志处的距离,以此作为定位标准。将该截面血管组织的IVUS影像分为外弹力膜、内膜、管腔及斑块。在病变近端和远端找到相对正常的血管截面作为参考血管截面,测量与CCTA相对应的定量参数[11-12]。IVUS的图像成像及测量由经验丰富的介入放射技师进行回顾性评估,评估人对冠状动脉造影及CCTA的结果不知情。
1.4 检测效果评估方法
根据患者置入支架内径将纳入病变(目标支架)分为A组(内径>3.0 mm)和B组(内径≤3.0 mm), 并根据病变所在节段(支架内部或支架边缘5 mm内)将A组/B组分为A1组/B1组(支架内部病变)和A2组/B2组(边缘病变), A1组加B1组为1组(病变所在节段在支架内部), A2组加B2组为2组(病变所在节段在支架边缘)。以IVUS为“金标准”,将CCTA检测所得定性及定量结果与IVUS检测结果进行比较,评估CCTA检测PCI术后支架内病变的准确性。
1.5 统计学分析
采用SPSS 25.0统计学软件进行数据处理,计量资料以(x±s)或[M(P25, P75)]表示,计数资料以[n(%)]表示。采用Pearson相关性检验分析CCTA定量检测结果与IVUS定量检测结果的相关性。采用Kappa检验分析CCTA、IVUS检查方法对支架狭窄与否判定结果的一致性,并进一步行四格表χ2检验比较两者间差异。P < 0.05为差异有统计学意义。
2. 结果
2.1 临床资料
本研究共选取符合标准的患者60例,平均年龄(61.80±9.60)岁,平均体质量指数(BMI)为(24.99±2.73) kg/m2, 其中男44例(73.33%)、女16例(26.67%); 选取置入支架的目标血管共计80处,分布在左主干(7处)、前降支(45处)、回旋支(16处)和右冠状动脉(12处),置入支架平均内径为(3.23±0.57) mm, 支架平均长度为(17.48±7.90) mm。
2.2 CCTA和IVUS定量检测参数结果的相关性分析
Pearson相关分析结果显示, CCTA的定量检测参数(MLD、MD、PL、MLA、EEMA、PB、PA和PV)结果均与IVUS呈显著正相关(P < 0.001), 见表 1。
表 1 冠状动脉CT血管造影与血管内超声定量检测参数结果的相关性分析(x±s)参数 冠状动脉CT血管造影 血管内超声 r P 最小管腔内径/mm 1.37±0.57 1.55±0.53 0.79 < 0.001 平均血管内径/mm 3.39±0.73 3.59±0.67 0.84 < 0.001 斑块长度/mm 17.18±10.86 16.49±10.17 0.83 < 0.001 最小管腔面积/mm2 2.09±1.45 2.46±1.47 0.82 < 0.001 外弹力膜面积/mm2 9.46±3.74 10.60±3.69 0.83 < 0.001 斑块负荷/% 76.95±14.22 75.48±14.02 0.81 < 0.001 斑块面积/mm2 7.37±3.35 8.14±3.40 0.84 < 0.001 斑块体积/mm3 126.23±103.45 133.69±103.40 0.79 < 0.001 2.3 支架内病变评估结果
IVUS检查共识别49处ISR、31处支架通畅, CCTA检查识别ISR 47处、33处支架通畅(假阳性3处)。
2.4 内径>3.0 mm支架内病变评估结果
A组41处中, IVUS检查共识别27处ISR, 14处支架通畅, CCTA检查共识别26处ISR、15处支架通畅(假阳性1处)。CCTA的特异性(92.86%)、灵敏性(92.59%)、准确性(92.68%)均较高,与IVUS结果一致性较好(Kappa=0.840, P < 0.001), 四格表χ2检验结果提示,两者间差异无统计学意义(P=0.817)。见表 2。
表 2 冠状动脉CT血管造影与血管内超声检查对A组(内径>3.0 mm)支架内再狭窄的诊断结果比较处 冠状动脉
CT血管造影血管内超声 合计 阳性 阴性 阳性 25 1 26 阴性 2 13 15 合计 27 14 41 2.5 内径≤3.0 mm支架内病变评估结果
B组39处中, IVUS检查共识别22处ISR、17处支架通畅, CCTA检查共识别21处ISR、18处支架通畅(假阳性2处)。CCTA的特异性(88.24%)、灵敏性(86.36%)、准确性(87.18%)低于A组中,与IVUS结果一致性一般(Kappa=0.741, P < 0.001), 四格表χ2检验提示,两者间差异无统计学意义(P=0.820)。见表 3。
表 3 冠状动脉CT血管造影与血管内超声检查对B组(内径≤3.0 mm)支架内再狭窄的诊断结果比较处 冠状动脉
CT血管造影血管内超声 合计 阳性 阴性 阳性 19 2 21 阴性 3 15 18 合计 22 17 39 2.6 CCTA对不同内径及不同节段支架内病变的识别结果
A组、B组的识别结果比较,差异无统计学意义(P=0.523); 1组、2组的识别结果比较,差异无统计学意义(P=0.212); A2组、B2组的识别结果比较,差异无统计学意义(P=0.484); A1组、B1组的识别结果比较,差异有统计学意义(P=0.011)。见表 4。
表 4 冠状动脉CT血管造影对各组支架内再狭窄的识别结果比较[n(%)]组别 n 支架内再狭窄 通畅 χ2 P A组 41 26(63.41) 15(36.59) 0.409 0.523 B组 39 21(53.85) 18(46.15) 1组 37 19(51.35) 18(48.65) 1.555 0.212 2组 43 28(65.12) 15(34.88) A1组 24 16(66.67) 8(33.33) 6.414 0.011 B1组 13 3(23.08) 10(76.92) A2组 17 10(58.82) 7(41.18) 0.490 0.484 B2组 26 18(69.23) 8(30.77) n为病变计数。 3. 讨论
既往研究[13]以CAG作为参考探讨CCTA诊断金属支架ISR的准确性,发现CCTA与CAG对ISR的诊断具有高度一致性,但由于偏心病变、支架伪影、造影剂充盈缺损等因素, CAG的准确性受到影响。IVUS用于金属支架内病变检测,具有CCTA无法企及的优势,其成像清晰、直观,可定量测量多种参数,还可观察到血管壁组织,对于再狭窄原因分析具有重要的临床意义[14]。本研究中, CCTA对支架内病变的定量检测结果与IVUS呈显著正相关,提示CCTA对病变处的测量准确性较高,即利用CCTA定量检测结果进一步分析所得结果是可靠的。
目前, CCTA已被广泛应用于ISR的诊断中,且具有风险性小、可重复性强的优点,但CCTA识别ISR尤其是内径较小支架ISR的准确性尚存争议。既往研究[15]提出, CCTA对内径≤3.0 mm支架内病变的检测准确性欠佳。但也有研究[16]证明,随着CCTA检测技术的进步,支架内径大小对诊断结果无明显影响。相关研究[17-19]指出,使用新一代DESs的重复支架置入术和药物球囊(DCB)是ISR最有效的治疗方法,但不同类型的ISR需选择不同的治疗方案。因此,进一步明确CCTA对不同内径ISR的诊断价值,对于CCTA的临床应用及ISR的治疗具有重要意义。本研究在对支架内径大小进行分类的基础上进一步对病变所在节段进行分类,并将CCTA检测结果与同一时期的IVUS判读结果进行比较,以期使ISR病变具体到节段,从而进一步明确CCTA的诊断价值。本研究结果显示, CCTA对内径>3.0 mm ISR的诊断特异性、灵敏性和准确性均较高,与IVUS判读结果无显著差异,与以往研究[20]结论一致; CCTA对内径≤3.0 mm ISR的诊断特异性、灵敏性和准确性低于内径>3.0 mm ISR。进一步分型后发现, CCTA对支架边缘5 mm内与支架内部ISR的诊断结果无显著差异,但对不同内径支架内部ISR的诊断结果存在显著差异[21-22]。由此提示, CCTA对较小内径支架内ISR的诊断结果并非完全不准确,其对支架边缘的ISR诊断可信度较高,但对支架内部的ISR检测结果则不够准确,需要使用更精确的腔内成像技术进一步明确诊断。本研究不足之处为纳入患者数量较少且为单中心研究,未来还需增大样本量开展多中心研究进一步证实该结论。
综上所述, CCTA是一种无创、方便的心血管影像技术,其对内径≤3.0 mm的支架内部ISR的诊断效果欠佳,对内径>3.0 mm的支架内部ISR和支架边缘ISR的诊断结果可信度较高,可应用于不同类型置入支架的检测中,在心血管病领域具有广泛的应用前景。
-
表 1 冠状动脉CT血管造影与血管内超声定量检测参数结果的相关性分析(x±s)
参数 冠状动脉CT血管造影 血管内超声 r P 最小管腔内径/mm 1.37±0.57 1.55±0.53 0.79 < 0.001 平均血管内径/mm 3.39±0.73 3.59±0.67 0.84 < 0.001 斑块长度/mm 17.18±10.86 16.49±10.17 0.83 < 0.001 最小管腔面积/mm2 2.09±1.45 2.46±1.47 0.82 < 0.001 外弹力膜面积/mm2 9.46±3.74 10.60±3.69 0.83 < 0.001 斑块负荷/% 76.95±14.22 75.48±14.02 0.81 < 0.001 斑块面积/mm2 7.37±3.35 8.14±3.40 0.84 < 0.001 斑块体积/mm3 126.23±103.45 133.69±103.40 0.79 < 0.001 表 2 冠状动脉CT血管造影与血管内超声检查对A组(内径>3.0 mm)支架内再狭窄的诊断结果比较
处 冠状动脉
CT血管造影血管内超声 合计 阳性 阴性 阳性 25 1 26 阴性 2 13 15 合计 27 14 41 表 3 冠状动脉CT血管造影与血管内超声检查对B组(内径≤3.0 mm)支架内再狭窄的诊断结果比较
处 冠状动脉
CT血管造影血管内超声 合计 阳性 阴性 阳性 19 2 21 阴性 3 15 18 合计 22 17 39 表 4 冠状动脉CT血管造影对各组支架内再狭窄的识别结果比较[n(%)]
组别 n 支架内再狭窄 通畅 χ2 P A组 41 26(63.41) 15(36.59) 0.409 0.523 B组 39 21(53.85) 18(46.15) 1组 37 19(51.35) 18(48.65) 1.555 0.212 2组 43 28(65.12) 15(34.88) A1组 24 16(66.67) 8(33.33) 6.414 0.011 B1组 13 3(23.08) 10(76.92) A2组 17 10(58.82) 7(41.18) 0.490 0.484 B2组 26 18(69.23) 8(30.77) n为病变计数。 -
[1] AOKI J, TANABE K. Mechanisms of drug-eluting stent restenosis[J]. Cardiovasc Interv Ther, 2021, 36(1): 23-29. doi: 10.1007/s12928-020-00734-7
[2] NAKAMURA D, DOHI T, ISHIHARA T, et al. Predictors and outcomes of neoatherosclerosis in patients with in-stent restenosis[J]. EuroIntervention, 2021, 17(6): 489-496. doi: 10.4244/EIJ-D-20-00539
[3] ANDREINI D, PONTONE G, MUSHTAQ S, et al. Diagnostic accuracy of coronary CT angiography performed in 100 consecutive patients with coronary stents using a whole-organ high-definition CT scanner[J]. Int J Cardiol, 2019, 274: 382-387. doi: 10.1016/j.ijcard.2018.09.010
[4] ECKERT J, RENCZES-JANETZKO P, SCHMIDT M, et al. Coronary CT angiography (CCTA) using third-generation dual-source CT for ruling out in-stent restenosis[J]. Clin Res Cardiol, 2019, 108(4): 402-410. doi: 10.1007/s00392-018-1369-1
[5] MUNNUR R K, ANDREWS J, KATAOKA Y, et al. Quantitative and qualitative coronary plaque assessment using computed tomography coronary angiography: a comparison with intravascular ultrasound[J]. Heart Lung Circ, 2020, 29(6): 883-893. doi: 10.1016/j.hlc.2019.06.719
[6] CONTE E, MUSHTAQ S, PONTONE G, et al. Plaque quantification by coronary computed tomography angiography using intravascular ultrasound as a reference standard: a comparison between standard and last generation computed tomography scanners[J]. Eur Heart J Cardiovasc Imaging, 2020, 21(2): 191-201.
[7] EIJSVOOGEL N G, HENDRIKS B M F, NELEMANS P, et al. Personalization of CM injection protocols in coronary computed tomographic angiography (people CT trial)[J]. Contrast Media Mol Imaging, 2020, 2020: 5407936.
[8] YUAN M Y, WU H, LI R X, et al. The value of quantified plaque analysis by dual-source coronary CT angiography to detect vulnerable plaques: a comparison study with intravascular ultrasound[J]. Quant Imaging Med Surg, 2020, 10(3): 668-677. doi: 10.21037/qims.2020.01.13
[9] OBAID D R, CALVERT P A, BROWN A, et al. Coronary CT angiography features of ruptured and high-risk atherosclerotic plaques: correlation with intra-vascular ultrasound[J]. J Cardiovasc Comput Tomogr, 2017, 11(6): 455-461. doi: 10.1016/j.jcct.2017.09.001
[10] KESARWANI M, NAKANISHI R, CHOI T Y, et al. Evaluation of plaque morphology by 64-slice coronary computed tomographic angiography compared to intravascular ultrasound in nonocclusive segments of coronary arteries[J]. Acad Radiol, 2017, 24(8): 968-974. doi: 10.1016/j.acra.2017.03.001
[11] GARCIA-GARCIA H M, COSTA M A, SERRUYS P W. Imaging of coronary atherosclerosis: intravascular ultrasound[J]. Eur Heart J, 2010, 31(20): 2456-2469. doi: 10.1093/eurheartj/ehq280
[12] CISMARU G, SERBAN T, TIRPE A. Ultrasound methods in the evaluation of atherosclerosis: from pathophysiology to clinic[J]. Biomedicines, 2021, 9(4): 418. doi: 10.3390/biomedicines9040418
[13] NOGOURANI M K, MORADI M, KHAJOUEI A S, et al. Diagnostic value of intraluminal stent enhancement in estimating coronary in-stent restenosis[J]. J Clin Imaging Sci, 2020, 10: 12. doi: 10.25259/JCIS_153_2019
[14] MALAIAPAN Y, LEUNG M, WHITE A J. The role of intravascular ultrasound in percutaneous coronary intervention of complex coronary lesions[J]. Cardiovasc Diagn Ther, 2020, 10(5): 1371-1388. doi: 10.21037/cdt-20-189
[15] DAI T, WANG J R, HU P F. Diagnostic performance of computed tomography angiography in the detection of coronary artery in-stent restenosis: evidence from an updated meta-analysis[J]. Eur Radiol, 2018, 28(4): 1373-1382. doi: 10.1007/s00330-017-5097-0
[16] LI Y H, YU M M, LI W B, et al. Third generation dual-source CT enables accurate diagnosis of coronary restenosis in all size stents with low radiation dose and preserved image quality[J]. Eur Radiol, 2018, 28(6): 2647-2654. doi: 10.1007/s00330-017-5256-3
[17] NEUMANN F J, SOUSA-UVA M, AHLSSON A, et al. 2018 ESC/EACTS guidelines on myocardial revascularization[J]. Eur Heart J, 2019, 40(2): 87-165. doi: 10.1093/eurheartj/ehy394
[18] NEUMANN F J, SOUSA-UVA M. "ten commandments" for the 2018 ESC/EACTS guidelines on myocardial revascularization[J]. Eur Heart J, 2018, 39(42): 3759. doi: 10.1093/eurheartj/ehy658
[19] EVORA P R B, ALBUQUERQUE A A S. The 2018 ESC/EACTS guidelines on myocardial revascularization still does not address the issue of disease-free saphenous vein grafts at the time of redo coronary artery bypass grafting[J]. Eur J Cardiothorac Surg, 2020, 57(1): 199-200. doi: 10.1093/ejcts/ezz009
[20] AMANUMA M, KONDO T, SANO T, et al. Assessment of coronary in-stent restenosis: value of subtraction coronary computed tomography angiography[J]. Int J Cardiovasc Imaging, 2016, 32(4): 661-670. doi: 10.1007/s10554-015-0826-4
[21] LI J, GUO M T, YANG X, et al. The usefulness of subtraction coronary computed tomography angiography for in-stent restenosis assessment of patients with CoCr stent using 320-row area detector CT[J]. Medicine, 2021, 100(51): e28345. doi: 10.1097/MD.0000000000028345
[22] 戴爱明, 杨中芳, 张守梅, 等. 冠状动脉造影及支架植入术患者的护理安全管理[J]. 实用临床医药杂志, 2019, 23(23): 40-42. doi: 10.7619/jcmp.201923012 -
期刊类型引用(3)
1. 严凯,薛维,沈丹丹. 冠状动脉CT血管成像定量参数对STEMI患者PCI后发生ISR的预测价值. 中国医师杂志. 2025(02): 307-311 .  百度学术
百度学术
2. 鲍利,罗晓花,徐峰,周国新. 冠状动脉CT血管造影对进行静脉输液的冠心病患者预后评估分析. 河北医药. 2024(22): 3400-3403 .  百度学术
百度学术
3. 谢春萍. CT血管成像对冠心病患者经皮冠状动脉介入治疗术后支架内再狭窄的诊断价值. 医疗装备. 2023(15): 84-87 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:

 苏公网安备 32100302010246号
苏公网安备 32100302010246号